Onderzoekers van de TU Eindhoven, Differ en MIT ontwikkelden een elektrode met honingraat-porieën om de elektrochemische reactie in de redox-flowbatterij te verbeteren. Het materiaal maakt de batterij efficiënter en breder inzetbaar. Bovendien is het nieuwe membraan makkelijker en goedkoper te produceren en geschikt voor grootschalige productie.
De onderzoeksresultaten zijn gepubliceerd in Advanced Materials.
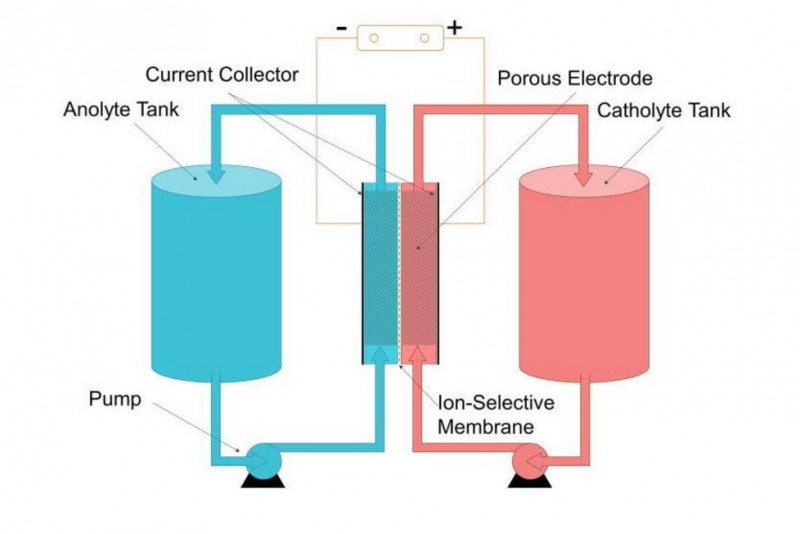
De redox-flow batterij ontleent zijn naam aan de vloeibare elektrolytoplossing die langs de reactiekamer stroomt en in aparte tanks is opgeslagen. De ene tank bevat een negatief geladen oplossing en in de andere tank zit de positief geladen oplossing.
In tegenstelling tot de lithium-ion variant, kunnen redox-flowbatterijen hun capaciteit (kWh) verhogen zonder het vermogen (kW) te verhogen, en omgekeerd. Door een grotere tank met elektrolytoplossing aan het systeem te koppelen, kun je zo heel simpel je capaciteit enorm uitbreiden.
Redox-flowbatterijen worden kostenconcurrerend als je ze heel lang kunt ontladen. Bovendien zijn redox-flow batterijen veel veiliger dan lithium-ion batterijen omdat de componenten vloeibaar en niet ontvlambaar zijn. Redox-flowbatterijen hebben ook een langere levensduur door het ontbreken van de intercalatiereacties die een negatieve invloed hebben op de stabiliteit.
Hoewel ze veelbelovend zijn, zijn de huidige kosten nog te hoog om op grote schaal te worden toegepast.
Wederzijdse uitsluiting?
Hoe sneller de elektronen stromen, hoe meer elektriciteit de batterij genereert. De elektrode van een redox-flowbatterij heeft daarom een poreuze structuur. Hoofdonderzoeker Antoni Forner-Cuenca van de TU/e: "Hoe groter de poriën, hoe makkelijker het elektrolyt er doorheen kan stromen en hoe lager het drukverlies. Maar als de poriën te groot zijn, doen we afstand van het grote oppervlak. Idealiter wil je dus een hoge stroomsnelheid én een groot reactieoppervlak."
Op dit moment gebruiken redox-flowbatterijen conventionele koolstofvezelelektroden. Deze zijn ontworpen voor lage temperatuur brandstofcellen. Maar deze elektroden zijn complex en duur om te produceren, en het productieproces maakt het moeilijk om de driedimensionale structuur van de poriën aan te passen aan de gewenste toepassing.
Membraanwetenschap biedt de oplossing
Forner-Cuenca: "We moesten terug naar de tekentafel om een beter presterende elektrode te ontwikkelen. Het ontwerp en de keuze van de materialen is daarbij volledig heroverwogen en verbeterd. Geïnspireerd door de membraanwetenschap en -technologie hebben we polymeerfasescheiding gebruikt om de elektrodestructuur te kunnen controleren.
"We beginnen daarbij met een vloeibare oplossing en twee polymeren. Door het materiaal onder te dompelen in water, krijg je een poreuze structuur. Eén van de polymeren lost namelijk op. Door te spelen met de samenstelling, het oplosmiddel, de temperatuur en andere parameters kunnen we de poreuze structuur van de elektrode zo nauwkeurig regelen. Het waren deze inzichten die de basis vormden voor ons nieuwe ontwerp."
Na talloze computersimulaties en experimenten wisten de onderzoekers een materiaal te ontwikkelen waarbij de poriegrootte en -vorm in de elektrode gemakkelijk kunnen worden aangepast, door de hoeveelheden oplosmiddel en polymeren te variëren. Forner-Cuenca: "Het fabricageproces van ons nieuwe materiaal is veel eenvoudiger en goedkoper, biedt een grotere veelzijdigheid en is gemakkelijker op te schalen dan bij conventionele elektrodenproductie. Het toont aan dat het wel degelijk mogelijk is om een elektrode te maken met zowel een gunstig bulk-elektronentransport als een groot reactieoppervlak."
Honingraatstructuur verhoogt efficiëntie
Een van de ontwikkelde structuren bleek een schot in de roos: de ‘honingraat’-elektrode met een combinatie van grote en kleine poriën. "Dat maakt deze structuur geschikt voor grootschalige energieopslag. De grote poriën garanderen de hoge stroomsnelheid, als ware het een snelweg, En de kleine poriën daartussen zorgen voor voldoende reactieoppervlak, de N-wegen."




